機能解析研究分野
沈 建仁 グループ
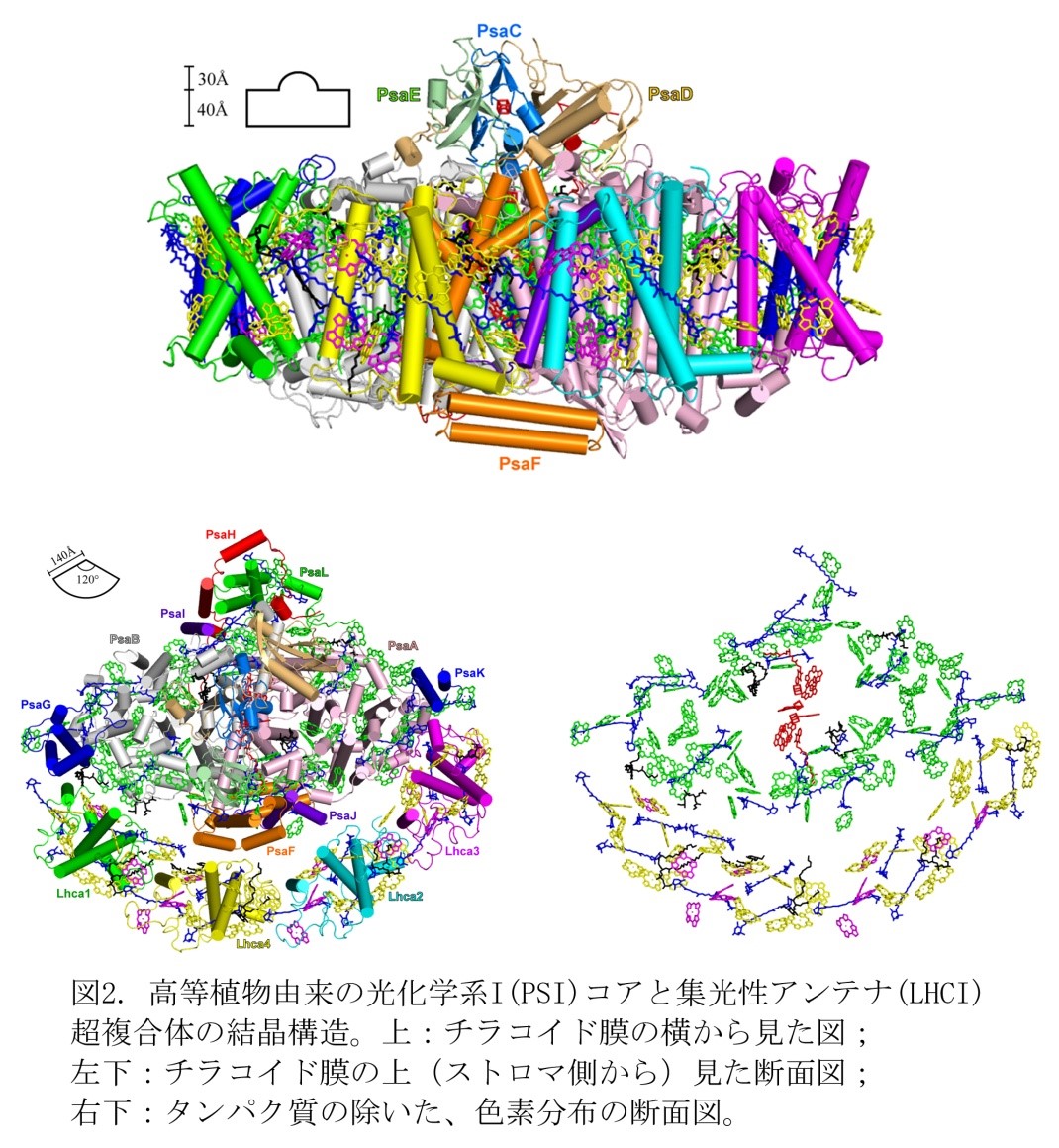
当研究分野では、植物や各種藻類が行う光合成の反応機構を、タンパク質の立体構造解析を通して解明する研究を行っています。これまで光化学系II (PSII)、光化学系I (PSI)という2つの光化学系巨大膜タンパク質複合体の構造を解析してきました。光化学系IIは光エネルギーを利用して水を分解し、酸素を放出する反応を触媒しており、我々は好熱性シアノバクテリア由来のPSIIの結晶構造を1.9 Åという世界最高分解能で解析し、水分解・酸素発生触媒(Mn4CaO5クラスター)の詳細な構造を解明しました(図1、Nature 473, 55-60 (2011))。さらにフェムト秒のX線自由電子レーザー施設SACLAを利用して、X線損傷を受けていない、天然状態のMn4CaO5クラスターの構造を解析し、水分解反応の機構に重要な知見を得ました(Nature 517, 99-103 (2015))。得られたPSIIのMn4CaO5クラスターの構造をもとに、共同研究により天然の触媒に近い形と性質を持つモデル化合物の合成にも成功しました(Science 348, 690-693 (2015))。また、光化学系IはPSIIの水分解由来の電子を用いて、二酸化炭素を糖に変換するために必要な還元力を作り出していますが、我々は高等植物のPSIコアと集光性アンテナ(LHCI)が結合してできたPSI-LHCI超複合体の結晶構造を解析し、LHCIからPSIコアへの光エネルギーの高効率移動の機構に重要な知見を得ました(図2、Science 348, 989-995 (2015))。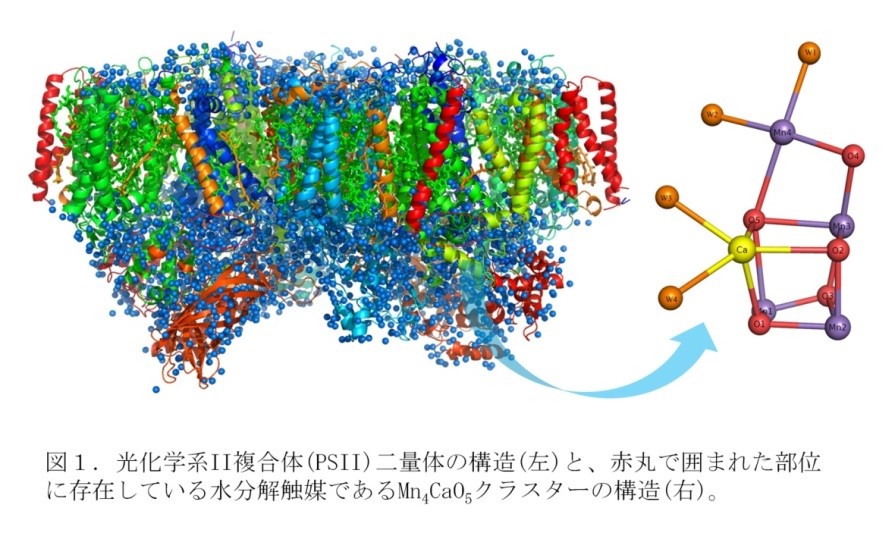
構造解析研究分野
菅 倫寛 グループ
人工光合成研究分野
鈴木 孝義 グループ
金属イオンに配位結合したある種の化合物を、水素イオン(H+:プロトン)の脱離と電子(e–)移動を共役させて酸化する方法は、プロトン共役電子移動(Proton-Coupled Electron Transfer: PCET)といわれ、生体内での多くの化学反応に関与していると考えられています。この原理を応用し、多くの有機物や水を低エネルギーで酸化する反応の開拓が試みられています。この研究で用いたテトラヒドロピリミジル基のピリミジル基への酸化には、4電子と4プロトンの移動が伴い、一般に強い酸化剤と高い反応温度が必要です。このテトラヒドロピリミジル基を含む有機物がルテニウム(Ru)イオンに結合した金属錯体では、金属イオンの酸化数が+2(RuII)の場合には解離が非常に難しかったN–H基が、ルテニウムを(RuIIIに)酸化すると容易にプロトンを脱離するようになった。この時、同時に有機物からの電子の放出とプロトンの脱離が連続的に起こり、テトラヒドロピリミジル基はピリミジル基に変換した。すなわち、ルテニウムイオンを一旦酸化し、塩基を加えることにより、プロトンと電子の放出が容易になり、温和な条件下でも有機物を4電子酸化することがわかった(図1)。また、最初の過程であるルテニウムイオンの酸化は電気化学的にも実現することができ、比較的低電位の電圧印加でこの酸化を実現できることもわかった。このように、通常は高い反応温度や強い酸化剤を必要とする多段階酸化反応を、金属イオンへの配位結合と塩基による水素イオンの脱離を組み合わせることにより低エネルギーで実現したこの反応は、人工光合成の鍵反応である水の酸化にも応用できると期待されます。(Inorganic Chemistry, 2013, 52, 10183–10190 (doi: 10.1021/ic401667v))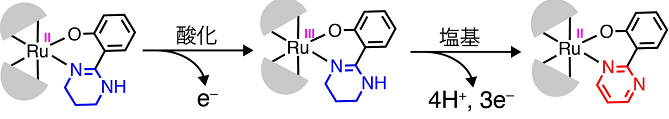
図1 ルテニウムイオンの酸化と塩基の添加によるテトラヒドロピリミジル基の4電子酸化反応
表面物理化学研究分野
山方 啓 グループ






