機能解析研究分野
沈 建仁 グループ
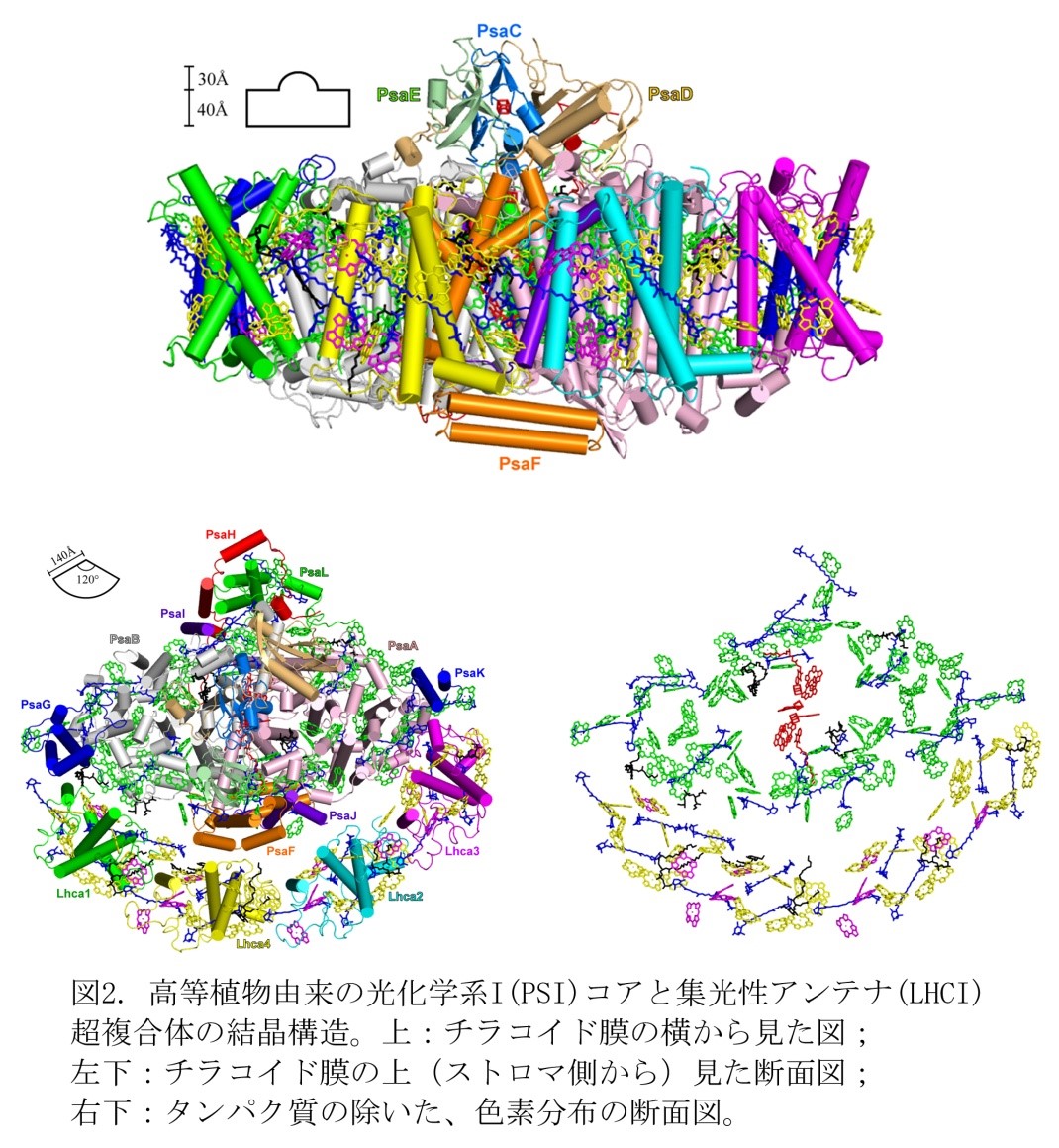
当研究分野では、植物や各種藻類が行う光合成の反応機構を、タンパク質の立体構造解析を通して解明する研究を行っています。これまで光化学系II (PSII)、光化学系I (PSI)という2つの光化学系巨大膜タンパク質複合体の構造を解析してきました。光化学系IIは光エネルギーを利用して水を分解し、酸素を放出する反応を触媒しており、我々は好熱性シアノバクテリア由来のPSIIの結晶構造を1.9 Åという世界最高分解能で解析し、水分解・酸素発生触媒(Mn4CaO5クラスター)の詳細な構造を解明しました(図1、Nature 473, 55-60 (2011))。さらにフェムト秒のX線自由電子レーザー施設SACLAを利用して、X線損傷を受けていない、天然状態のMn4CaO5クラスターの構造を解析し、水分解反応の機構に重要な知見を得ました(Nature 517, 99-103 (2015))。得られたPSIIのMn4CaO5クラスターの構造をもとに、共同研究により天然の触媒に近い形と性質を持つモデル化合物の合成にも成功しました(Science 348, 690-693 (2015))。また、光化学系IはPSIIの水分解由来の電子を用いて、二酸化炭素を糖に変換するために必要な還元力を作り出していますが、我々は高等植物のPSIコアと集光性アンテナ(LHCI)が結合してできたPSI-LHCI超複合体の結晶構造を解析し、LHCIからPSIコアへの光エネルギーの高効率移動の機構に重要な知見を得ました(図2、Science 348, 989-995 (2015))。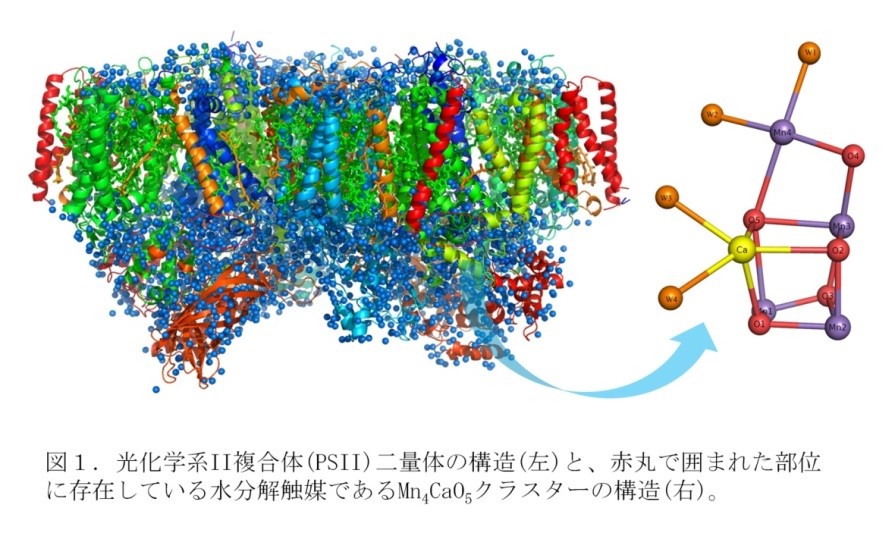
構造解析研究分野
菅 倫寛 グループ
当研究分野では、X線自由電子レーザー(XFEL)や放射光X線、クライオ電子顕微鏡などの最先端構造解析技術を駆使し、光合成の水分解反応を担う光化学系Ⅱの構造とその動的変化を解明してきました(Science 366, 334-338, 2019, Nature 626, 670-677, 2024)。また、植物の膜輸送体がどのように機能するのかを原子レベルで明らかにしました(Nature Communications 12, 6236, 2021、PNAS 122, e2501933122, 2025)。 巨大タンパク質複合体である光化学系IIの瞬間的な構造変化を捉えるには、時間分解構造解析が不可欠です。この手法により、酸素発生反応や光エネルギー変換の仕組みを、静的な構造ではなく「進行中の反応」として理解することが可能になります。 本研究分野では、放射光施設SPring-8やXFEL/SACLAといった国内外の大型研究施設に加え、岡山大学のクライオ電子顕微鏡およびクライオFIB-SEMを活用し、動的な生命反応の立体構造や、細胞内におけるタンパク質のありのままの振る舞いを観察しています。これらを統合的に用いる研究体制は、世界的にも最前線に位置するものです。 構造生命科学は、もはや「静止した形を見る」学問ではありません。「生きた反応を動画のように捉える」学問へと進化しています。このアプローチは、人工光合成の実現、新規触媒設計、創薬標的の開拓、さらには新たなバイオテクノロジーの創出へと直結します。
図1. 光化学系Ⅱにおける光合成反応の動的な構造変化
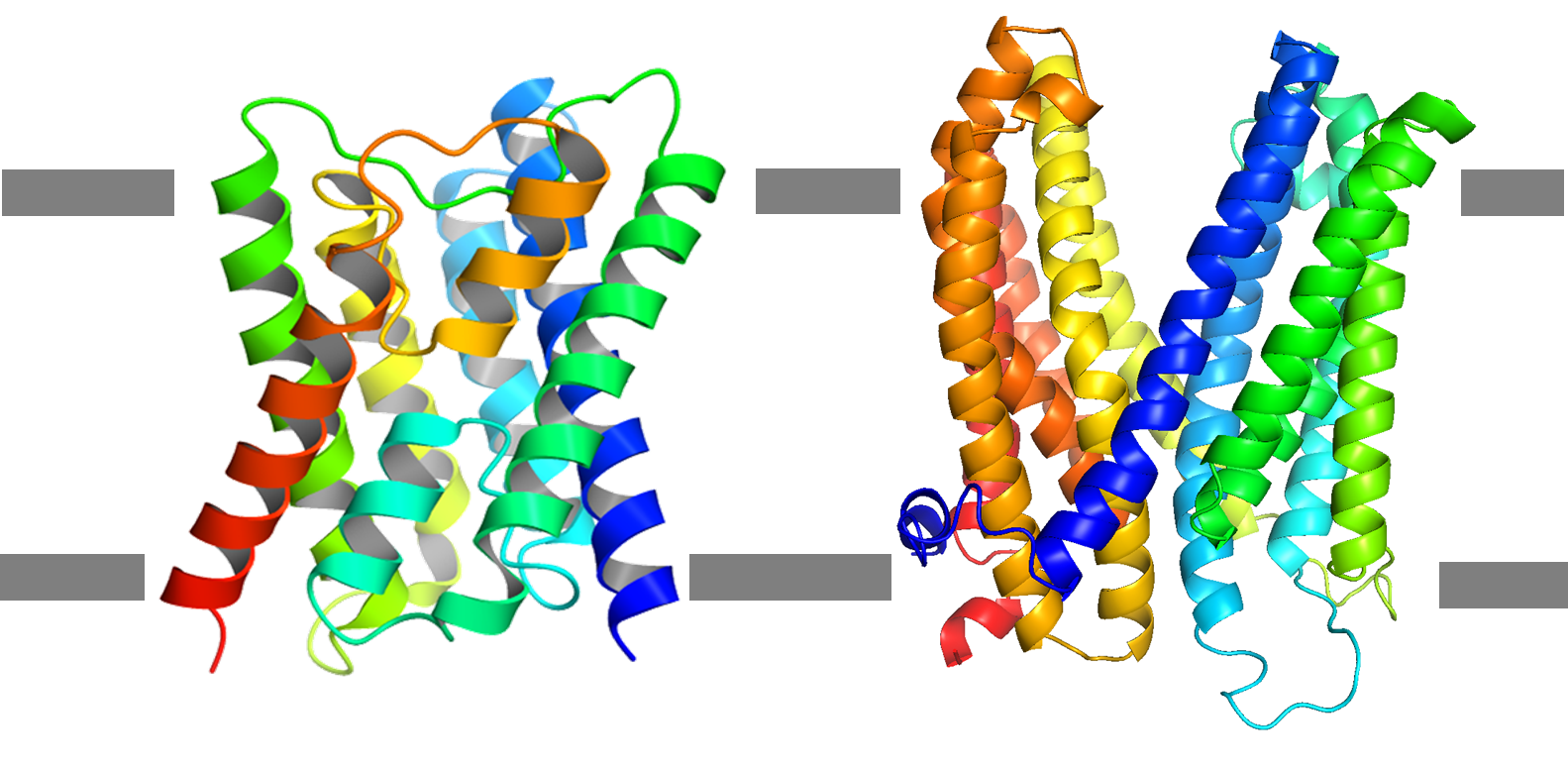
図2. イネのケイ酸輸送体Lsi1(左)とオオムギのクエン酸輸送体AACT1(右)
人工光合成研究分野
鈴木 孝義 グループ
金属イオンに配位結合したある種の化合物を、水素イオン(H+:プロトン)の脱離と電子(e–)移動を共役させて酸化する方法は、プロトン共役電子移動(Proton-Coupled Electron Transfer: PCET)といわれ、生体内での多くの化学反応に関与していると考えられています。この原理を応用し、多くの有機物や水を低エネルギーで酸化する反応の開拓が試みられています。この研究で用いたテトラヒドロピリミジル基のピリミジル基への酸化には、4電子と4プロトンの移動が伴い、一般に強い酸化剤と高い反応温度が必要です。このテトラヒドロピリミジル基を含む有機物がルテニウム(Ru)イオンに結合した金属錯体では、金属イオンの酸化数が+2(RuII)の場合には解離が非常に難しかったN–H基が、ルテニウムを(RuIIIに)酸化すると容易にプロトンを脱離するようになった。この時、同時に有機物からの電子の放出とプロトンの脱離が連続的に起こり、テトラヒドロピリミジル基はピリミジル基に変換した。すなわち、ルテニウムイオンを一旦酸化し、塩基を加えることにより、プロトンと電子の放出が容易になり、温和な条件下でも有機物を4電子酸化することがわかった(図1)。また、最初の過程であるルテニウムイオンの酸化は電気化学的にも実現することができ、比較的低電位の電圧印加でこの酸化を実現できることもわかった。このように、通常は高い反応温度や強い酸化剤を必要とする多段階酸化反応を、金属イオンへの配位結合と塩基による水素イオンの脱離を組み合わせることにより低エネルギーで実現したこの反応は、人工光合成の鍵反応である水の酸化にも応用できると期待されます。(Inorganic Chemistry, 2013, 52, 10183–10190 (doi: 10.1021/ic401667v))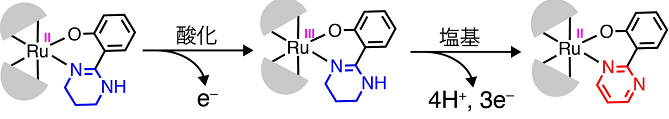
図1 ルテニウムイオンの酸化と塩基の添加によるテトラヒドロピリミジル基の4電子酸化反応
表面物理化学研究分野
山方 啓 グループ
当研究室では、光触媒の高活性化に向けて、光励起キャリア(電子・正孔)の生成、移動、反応、再結合の機構解明に基づく材料設計指針の構築を進めています。エネルギー・環境問題の解決に向けて光触媒への期待は大きい一方、実用化にはさらなる高活性化が必要です。私たちは、経験的な材料探索だけでなく、「なぜ高活性なのか/なぜ失活するのか」を時間軸で可視化して理解することが、性能向上への最短ルートであると考えています。この目的のために、粉末光触媒表面に適用可能な独自の時間分解分光装置を構築し、これまで観測が難しかった固体表面での電荷移動過程や分子反応過程の実時間観察を行ってきました(図1)。これにより、水分解光触媒における電荷移動の律速過程、欠陥やドーパントがキャリア寿命・反応性に及ぼす効果、助触媒や異種接合界面による電荷分離促進機構などを明らかにし、高活性化のための具体的な設計指針を提案しています(Angew. Chem. Int. Ed., 64, e202419624, 2025)。さらに近年は、光触媒・光電極に加えて有機太陽電池などの光機能材料にも対象を広げ(Chem. Sci., 15, 12686–12694, 2024)、時間分解分光を基盤とした機構解明を通じて、新しい光エネルギー変換材料・デバイスの創出を目指しています。
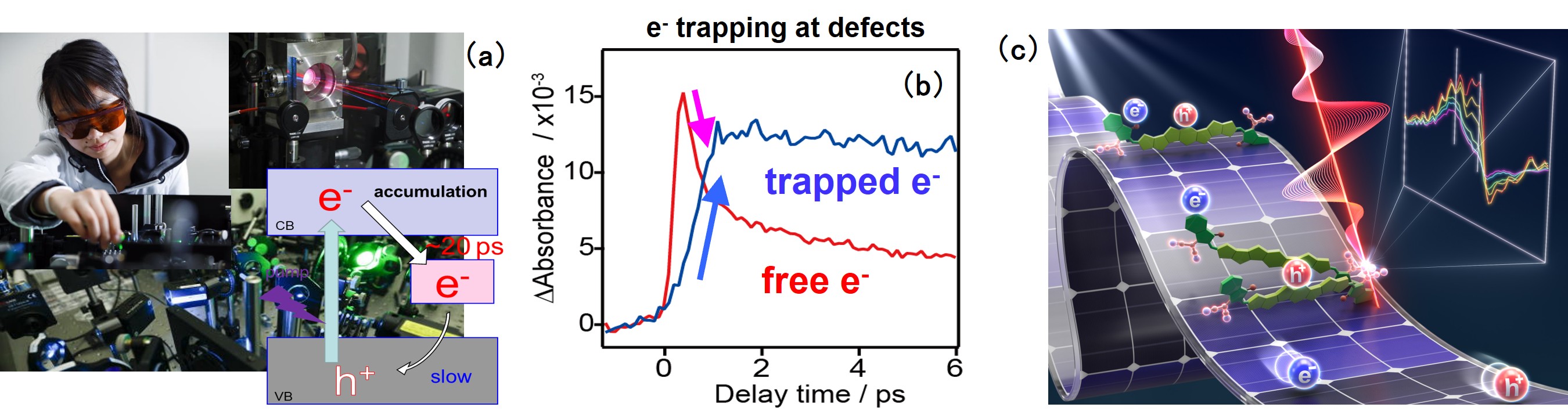
図1 フェムト秒時間分解可視近中赤外レーザー分光装置を使った実験の様子(a)と光触媒中の伝導帯電子が欠陥に捕捉される様子(b)。また、有機太陽電池の分子内・分子間で電荷分離過程を解明。






